Анотація
Дистанційний курс
«Хімічні реакції та закономірності їх перебігу»
призначений для учнів 9-х класів з поглибленим вивченням хімії.
Курс складено за програмою для загальноосвітніх навчальних закладів з поглибленим вивченням хімії, затвердженою наказом МОН України від 17.07.2015 № 983.
Згідно з програмними вимогами учні опанують:
- окисно-відновні реакції. Найважливіші окисники і відновники;
- поняття про енергетику хімічних реакцій, закон збереження енергії, його значення для хімічних процесів;
- перетворення енергії під час хімічних реакцій, внутрішню енергію і тепловий ефект, поняття про ентальпію;
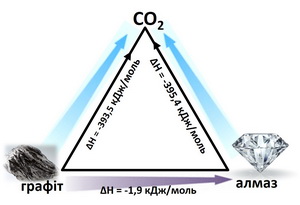
- екзо- та ендотермічні реакції, термохімічні рівняння, закон Гесса;
- поняття про хімічну кінетику, швидкість хімічної реакції;
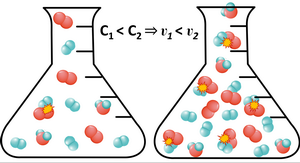
- залежність швидкості реакції від концентрації реагуючих речовин, закон діючих мас;
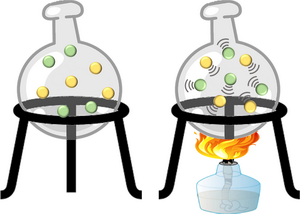
- залежність швидкості реакції від температури і природи реагуючих речовин, поняття про енергетичний бар’єр, активований комплекс, енергію активації;
- залежність швидкості реакції від наявності каталізатора і від площі поверхні зіткнення реагуючих речовин;
- каталіз. каталізатори та інгібітори,теорію проміжних сполук, загальні відомості про гомогенний та гетерогенний каталіз;
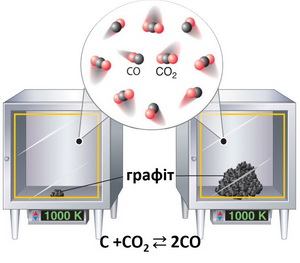
- хімічну рівновагу, оборотні та необоротні реакції, константу хімічної рівноваги;
- порушення рівноваги внаслідок зміни концентрації будь-якої з речовин, що беруть участь в реакції, тиску і температури, принцип Ле Шательє.
навчаться:
- наводити приклади ендо- та екзотермічних, оборотних та необоротних, каталітичних та некаталітичних, окисно-відновних та без зміни ступеня окиснення хімічних елементів, ланцюгових реакцій;
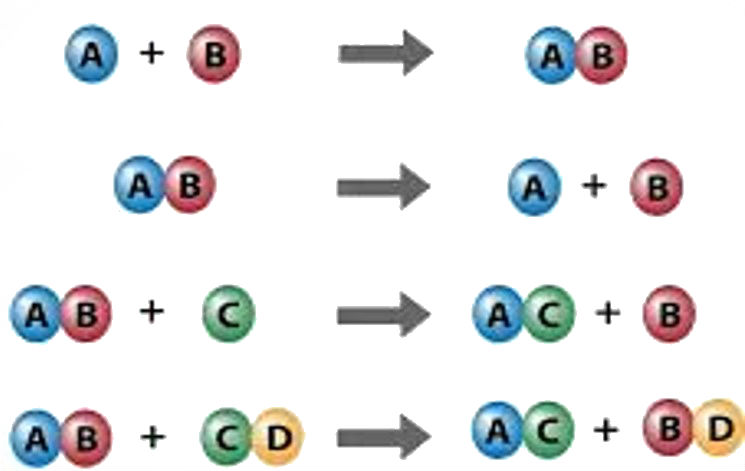
- розрізняти реакції сполучення, розкладу, заміщення, обміну;
- складати рівняння хімічних реакцій різних типів: окисно-відновні, термохімічні та йонно-молекулярні;
- класифікувати реакції за різними ознаками;
- пояснювати суть закону збереження енергії, закону Гесса, закону діючих мас, принципу Ле-Шательє, понять ентальпії, енергетичного бар'єру, енергії активації, каталізу;
- обґрунтовувати залежність швидкості гомогенної та гетерогенної реакціх від концентрації реагентів, температури, площі поверхні, тиску тощо, зміщення стану хімічної рівноваги в результаті зміни концентрації, тиску, температури;
- обчислювати тепловий ефект хімічної реакції, швидкість реакції за законом діючих мас, зміну швидкості реакції зі зміною температури за правилом Вант-Гоффа, константу рівноваги за значеннями рівноважних концентрацій реагентів;
- оцінювати значення хімічних реакцій різних типів.
На виконання вимог програми курс розподілений на 8 занять, які структуровані таким чином.
Кожне заняття містить наступні модулі:
- урок, який складається з набору сторінок з теоретичним матеріалом і сторінок з тестовими питаннями для закріплення знань;
- презентацію;
- приклади розв’язання завдань;
- завдання для самостійного розв’язування;
- тест самоконтролю.
До переважної кількості занять пропонуються відеофрагменти.
Тема закінчується контрольним тестом, що містить завдання різних типів за усіма вивченими темами.
Вимоги до навчального рівня підготовки учнів.
Успішне опанування кусу передбачає володіння учнями умінь:
характеризувати властивості оксидів, основ, кислот, солей;
складати формули цих сполук і відповідні рівняння реакцій;
обчислювати за рівняннями хімічних реакцій масу, кількість речовини та об’єм газу (н. у.) за відомою масою, кількістю речовини, об’єму одного з реагентів чи продуктів реакції; молярну концентрацію розчиненої речовини у розчині.
Даний курс є цікавим не лише для учнів природничого профілю навчання, а й для тих, хто готується до олімпіад з хімії та працює у Малій академії наук України.